トップページ > 診療科・部門 > 診療科 > トラベルクリニック > 5.エムポックスに対する曝露前予防の研究
5.エムポックスに対する曝露前予防の研究
電話番号:
エムポックス予防に関する臨床研究への参加を希望される方へ
現在、国立国際医療研究センター(NCGM)等では、エムポックスに対する予防が薬事承認されている、ワクチン(LC16)を用いた曝露前予防に関する臨床研究をエムポックスの感染リスクが高い成人の方を対象に実施しています。
また、研究計画が変更され、NCGMから研究参加登録をされたHIV陽性者を対象に、ワクチン接種の前後に2回の採血を行い、ワクチン接種による抗体の上昇を追加して評価する研究に参加いただけるようになりました。
対象者の方には、LC16ワクチンの接種前に、追加評価への参加についてご案内差し上げることがあります。
当該臨床研究では、研究への参加に当たって、事前の医学的評価により、選択基準に該当すること及び除外基準に非該当であること、を確認する必要があること、
評価に必要となる情報収集及び診療等の対応を確実に実施する必要があることから、原則として、研究実施医療機関に通院されている方を対象としています。
一方で、研究実施期間に通院されていない方で当該臨床研究に参加を希望される方に対して、NCGMでは、研究に参加するために必要となる「事前の医学的評価のための診療」を下記のように提供させていただきます。
研究について
研究では、エムポックスに対するワクチン(LC16)を用いて、エムポックスに対する有効性及び安全性等を確認します。
研究は、以下のような体制で実施します。
- 研究課題名 乾燥細胞培養痘そうワクチンLC16によるエムポックス発症予防効果を検討する無作為化比較試験
- 研究代表医師 国立国際医療研究センター 国際感染症センター
トラベルクリニック医長 氏家 無限 - 研究期間 2023年度末まで(予定)
- 被検者登録期間 2023年6月1日から2023年10月6日までの予定
- 共同研究機関 パーソナルヘルスクリニック
しらかば診療所
プライベートケアクリニック東京 新宿院・東京院
東京都立墨東病院
東京都立駒込病院
東京医科大学病院 - エムポックスに対するワクチン(LC16)について
LC16は、日本で開発され1980年に天然痘に対して薬事承認されました。その後、2022年8月には、エムポックスに対する予防適応が追加承認されています。
一般名: 乾燥細胞培養痘そうワクチンLC16「KMB」
製造販売: KMバイオロジクス株式会社
エムポックスに対するワクチン相談(1回目の受診)
本臨床研究に参加するためには、研究の選択基準及び除外基準に関する医学的な適格性を確実に評価するため、研究実施医療機関を事前に受診することが求められます。
加えて、研究計画に基づいた予防接種後の安全性及び有効性に関する評価の対応に確実にご協力いただく必要があります。
研究に参加することを目的に、評価のための事前受診する場合には、初診料に相当する2,880円(税抜)を、初回受診時にいただくことを、予めご了承ください(他の診療目的で受診した際に、研究へ参加する場合には、当該費用は免除となる場合があります)。
評価後、研究に参加することになった方には、改めて規定の接種日をご案内した上で、別日にエムポックスに対するワクチン(LC16)の接種を目的に受診いただきます。
本研究の参加目的に受診を希望される場合には、まずはお電話にて1回目の予約をしてください。
- 研究参加のための評価を目的とした事前受診(1回目 受診)
- エムポックスに対するワクチン(LC16)接種のための受診(2回目 受診)
受診者の方にお願いする対応
※ HIV感染者の方:受診時に診断名、治療内容、6カ月以内のCD4陽性細胞数の値等、医学的な適格性評価に必要な情報をかかりつけ医療機関からの紹介状等によって持参いただく必要があります。受診の前に予め紹介状をご用意ください。※ その他の方:研究規定に沿って、スクリーニング検査を受けていただき、研究参加登録前に結果を確認いただく必要があります。
当院でHIVスクリーニング検査をお受けになる際には、別途費用負担約3000円(税抜)が発生する他、検査結果を確認するまで、当日1時間から1時間半程度、お待ちいただきます。
4カ月以内に実施したHIVスクリーニング検査の結果を確認できる証明書(氏名、実施機関、実施日、実施検査内容の情報を含む)
また、受診いただいた場合でも、研究に参加するための選択基準及び除外基準に関する評価に基づき、研究に参加いただけない場合もあります
1回目受診の際の注意事項:
- 通常の診療の予約とは異なるため、予約受付を行う日時を限定させていただきます。診療枠には上限があることについてご了承ください。
- 通常のトラベルクリニックの受付にご連絡いただいても、研究参加のための受診はできませんのでご注意ください。
- 研究への参加を希望する方への対応を行う診療枠であるため、現時点で、その他の予防接種の相談等には対応できません。必要時には、別の通常診療の予約を取っていただく必要があります。
- 研究に参加いただく際には、調査期間中における調査票や問診票等の回答に、ご協力いただくことが求められます。ご理解の上、ご予約ください。
- このページ下部に、研究に関して説明する動画を用意しています。また、研究に関する説明書のPDFを掲載しています。あらかじめ動画を視聴し、説明書を読んでからご来院いただけると、研究に関する説明や手続きがスムーズに実施できますので、ご協力ください。
予約
受付電話番号:050-5369-6550(本研究のトラベルクリニック受診のための予約専用番号)
電話の受付時間は平日9:30 から 15:30までです。(土曜・日曜・祝日は対応しておりませんのでご注意下さい)
・2023年8月2日より受診のための電話受付時間を拡大しております。
・本研究に対するお問合せも本受付電話番号にて受け付けております。
・トラベルクリニックの受診可能日は毎週金曜日13:20~14:20のみとなっております。詳しくは、エムポックスに対するワクチン相談(1回目の受診)をご参照下さい。
・予約可能な日時は、2023年10月6日までの毎週金曜日です。(受診日によって痘そうワクチン接種候補日が変わります。詳しくは電話にてお問合せ下さい。)
注意:研究参加希望者のための特別な対応であるため、それ以外の日時では予約を受けて受けていません。
診療時間
1回目の受診
評価のための事前受診:金曜日、午後13:20~14:20(最終受付)
2回目の受診
LC16接種のための受診:規定された特定の日付の水曜日 9:30~12:00、13:00~16:00(研究参加者には受診可能な日程が2日提示されます)
注意:提示された日程に対する予約はウェブを通じて事前に予約を取っていただく必要があります。
被験者の適格性確認チャート
研究に参加することができるかどうかを確認するための簡略図を下記に示します。最終的な判断等については、診療で決定されることにご注意ください。
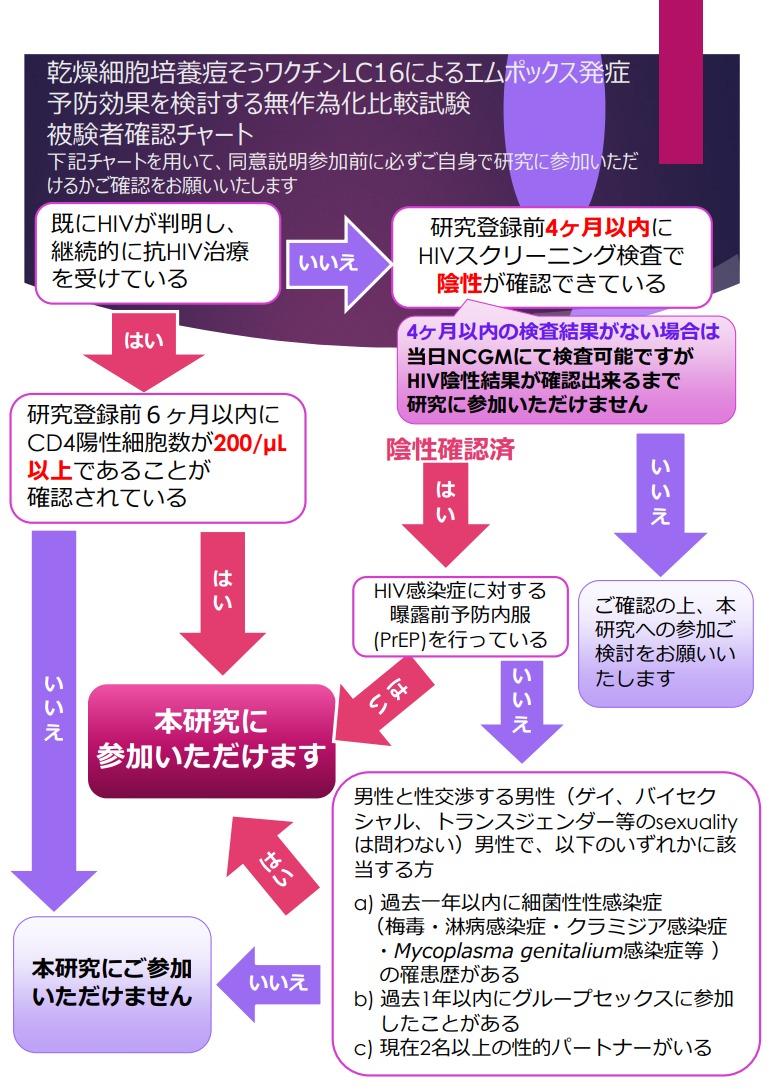
ただし、下記に当てはまる方は研究に参加いただけません。
1. エムポックスの既往歴がある人
2. 2022年位以降にエムポックスワクチンの接種歴がある人
3. エムポックスと診断された方と14日以内に中等度以上の接触歴がある人(曝露後予防の対象者)
4. 免疫不全状態にある人
5. エムポックスワクチンの成分に対するアナフィラキシー反応を呈したことが明らかな人
6. 妊娠している人及び妊娠している可能性のある人、等
エムポックスに対するワクチン接種(2回目の受診)
接種の概要
- 来院時間:予約時間の10分前
- 予防接種の診療を行うに当たって、3100円(税込み)の費用を事前に徴収させていただきます。※カード及び電子決済不可であるため、予め現金をご用意ください
- 当日持参するもの:1回目の受診時にお渡しする、ワクチン問診票及び接種時(Visit 2)の調査票(当日記載したもの)、研究参加カード、健康保険証(保険診療が必要になった際のため)。
注意事項
- 来院時には、「再来受付機」にて受付をしていただく必要はありません。1回目の受診時、研究登録後にお渡しする接種当日についてのご案内を参考に、直接ワクチン接種会場へお越しください。
- 接種前には事前の手続きがあるため、予約時間10分前までに来院してください。
- 接種時間は、受付順番等により前後する場合があります。
- 接種後30分間は、体調観察のため院内でお過ごしください。
- 接種後15分間は、接種後の注意等の動画を視聴いただき、接種会場でお過ごしください。
- 当日、家を出る前に熱を測り、熱がある場合は必ずご連絡ください。
- ワクチンの安全性及び有効性を評価するため、接種を受けた方には接種後の体調変化に関する調査票等をお渡しします。定められた日程でウェブから必要事項を回答下さい。
- 体調の変化に対して、受診を検討する際には、研究参加手続きをした医療機関にご連絡ください(研究参加カードに連絡先の記載があります)。
参考情報(LC16ワクチンの接種方法等)
NCGM 予防接種支援センター「天然痘(痘そう)及びエムポックスに対するワクチンについて」
研究に関連してかかる費用
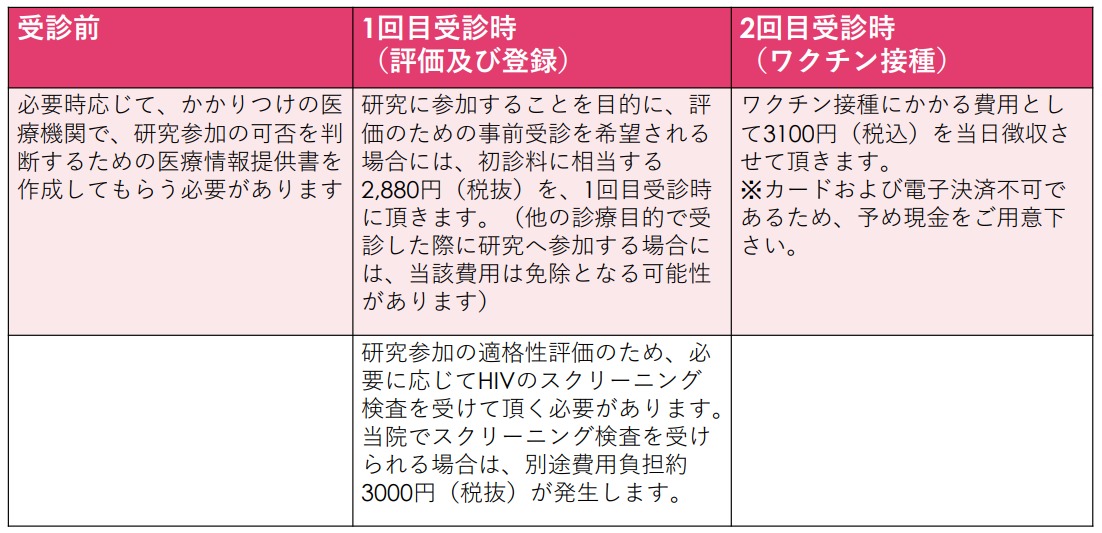
研究の全体図
簡易的な研究の全体図を下記に示します。詳細については、適宜、ご確認ください。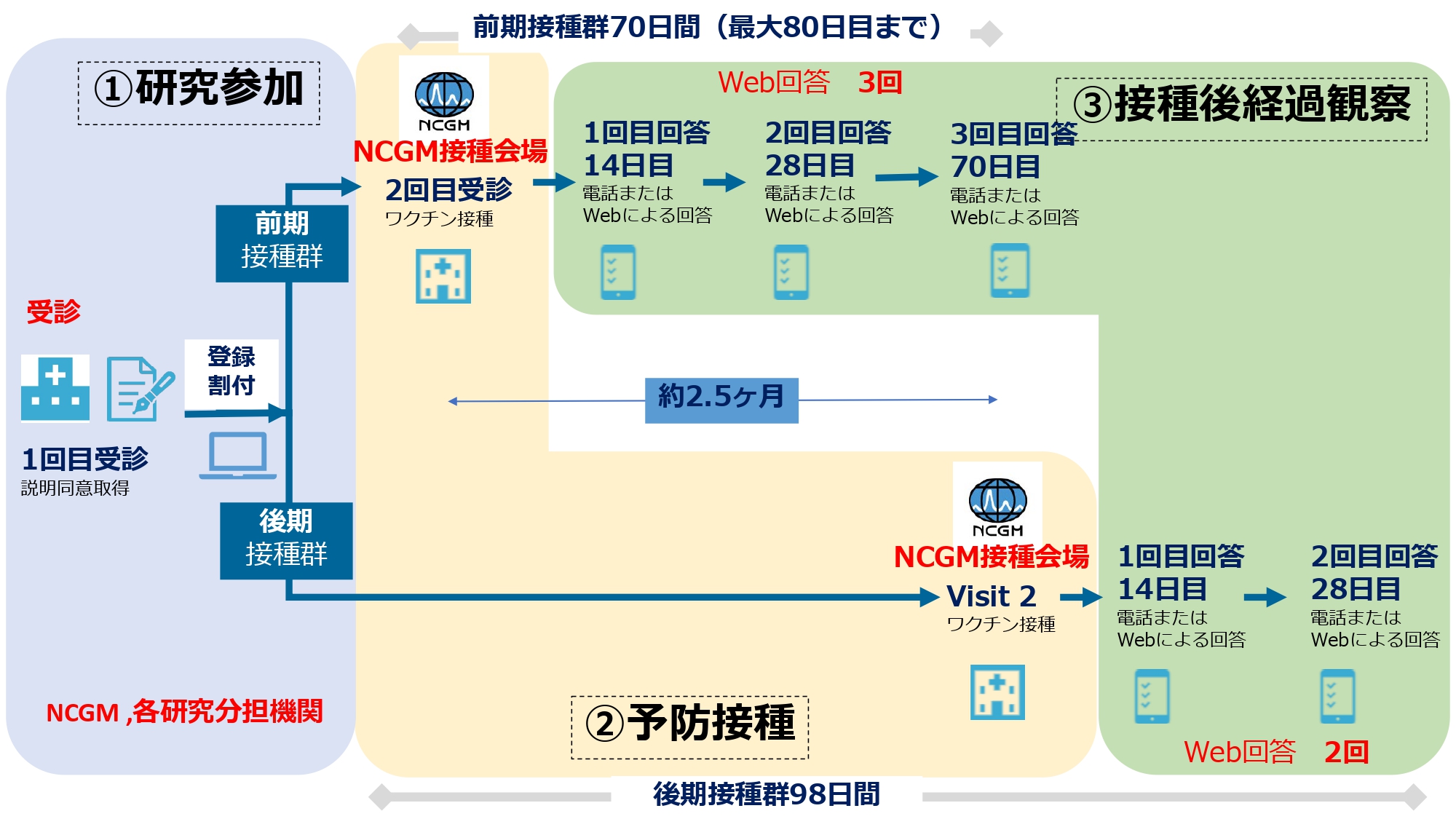
研究に関する説明書・説明ビデオ
エムポックスに対するワクチンの接種を希望する方は、予め以下の説明ビデオを視聴し、説明書を読んでから来院いただくと、手続きがスムーズです。
説明文書(参考資料)
「乾燥細胞培養痘そうワクチンLC16によるエムポックス発症予防効果を検討する無作為化比較試験」の研究への参加について
「乾燥細胞培養痘そうワクチンLC16によるエムポックス発症予防効果を検討する無作為化比較試験」における免疫原性評価のための血液検査について
※こちらの研究は、HIV陽性で国立国際医療研究センターかかりつけの方(本研究参加のためにトラベルクリニックを受診した方も含む)を対象とした研究です。
実際の資料については、受診当日にお渡しします。
説明ビデオ https://www.youtube.com/watch?v=CB5ac7yUQ9A&feature=youtu.be
エムポックスに対するワクチンに関する研究のQ&A
Q1. LC16ワクチンは生ワクチンであるため、HIV感染者に接種することはできますか?
A1. 弱毒生ワクチンは活動性のある癌患者、移植患者、免疫抑制剤で治療を受けている人、免疫不全者(CD4陽性細胞数が200/μl未満のHIV感染者)等では、接種を受けていただく事ができません(WHO, ガイダンス)。
そのため、本研究ではHIV感染者の方は、ART治療中で安定していること、半年以内にCD4陽性細胞数が200/μl以上であることを確認した上で、研究に参加いただきます。
同様に、LC16ワクチン以外の弱毒生ワクチン(麻疹、風疹など)についても、CD4陽性細胞数が200/μl以上であることが、接種の適応となる条件とされています(PMCID: PMC5595779)。
Q2. 欧米で使用されている別のエムポックスに対するワクチン(MVA-BN)の接種を受けることはできますか?
A2. MVA-BNワクチンは国内で承認されておらず、世界的に供給も限られている等の理由から、接種を受けることは難しいと考えられます。
Q3. LC16ワクチンの接種を受ける日時は研究参加者の都合で選べますか?
A3. コンピューターにより無作為に早めの日程で接種を受ける人と遅めの日程で接種を受ける人に別れますが、これを選ぶことはできません。
また、接種を受けることが可能な日程は最後の組み入れを除き、予め定められた接種機関のうち、2日間を提示させていただき、そこから選択していただきます(できるだけ直近の接種日を選んでいただくようにお願いしています)。
受診時間は、特定の時間に受診者が重ならないように、午前と午後の空いている診療枠から選択してご自身で予約を取っていただきます。
Q4. 研究に参加すると、通常の診療に加えて、どんなことを追加で求められますか?
A4. 研究では、LC16ワクチン接種後およそ14日後、28日後、70日後に、ウェブを通じて体調等の変化を報告していただくことをお願いしています。報告の内容は、症状の種類、程度、開始日と終了日、医療機関受診の有無などです。
その他、研究実施期間に、もしエムポックス罹患が疑われる、または診断されるなどした場合、何らかの理由で医療機関に入院するなどの事象が生じた場合には、適宜、登録医療機関にご連絡いただく事をお願いしています。
Q5. LC16ワクチンの接種後に体調が悪くなったらどうすれば良いですか?
A5. 体調の変化を感じた場合は、必要に応じて研究登録医療機関等を受診し、医師の診察を受けてください。また、その内容は、調査期間以内であれば、ウェブ等を通じて報告してください(電話での連絡先は研究参加カードに記載されています)。
Q6. 幼少期に天然痘ワクチンの接種歴がある年代だが、研究に参加することは可能ですか?
A6. 幼少期に天然痘ワクチンの接種歴がある方も、その他の研究参加に関する基準に問題がなければ、研究に参加していただけます。ただし、2022年以降にエムポックス予防目的にワクチン接種を受けたことがある方は研究に参加していただく事ができません。
Q7. 最近、他のワクチン接種を受けたことがあるが(受ける予定だが)、研究に参加することは可能ですか?
A7. LC16ワクチンは弱毒生ワクチンであるため、他の弱毒生ワクチンと4週間以上の接種間隔を置く必要があります。不活化ワクチンはこの限りではありません。
また、新型コロナウイルスワクチンの接種の際には、臨時接種実施要領において、原則として、前後2週間の接種間隔を置くことが求められています。
Q8. この研究は治験ですか?
A8. 本研究は既に安全性及び有効性が認められて薬事承認されたLC16ワクチンの更なる臨床データを評価するための研究であり、製薬企業が医薬品の開発のために行う臨床治験ではありません。
Q9. LC16ワクチンの詳しい安全性や有効性のデータはどこを見れば良いのか?
A9. 2022年8月時点での安全性及び有効性のデータは、厚生労働省の審議会資料に分かりやすくまとまっていますので、参考にされて下さい。